醫(yī)用低溫保存箱注冊(cè)技術(shù)審查指導(dǎo)原則
本指導(dǎo)原則旨在指導(dǎo)注冊(cè)申請(qǐng)人對(duì)第二類醫(yī)用低溫保存箱產(chǎn)品注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫��,同時(shí)也為技術(shù)審評(píng)部門審評(píng)注冊(cè)申報(bào)資料提供參考�。
本指導(dǎo)原則是對(duì)醫(yī)用低溫保存箱的一般要求�����,申請(qǐng)人應(yīng)依據(jù)產(chǎn)品的具體特性確定其中內(nèi)容是否適用�����,若不適用���,需具體闡述理由及相應(yīng)的科學(xué)依據(jù)����,并依據(jù)產(chǎn)品的具體特性對(duì)注冊(cè)申報(bào)資料的內(nèi)容進(jìn)行充實(shí)和細(xì)化���。
本指導(dǎo)原則是供申請(qǐng)人和審查人員使用的指導(dǎo)文件�����,不涉及注冊(cè)審批等行政事項(xiàng)����,亦不作為法規(guī)強(qiáng)制執(zhí)行,如有能夠滿足法規(guī)要求的其他方法����,也可以采用,但應(yīng)提供詳細(xì)的研究資料和驗(yàn)證資料���。應(yīng)在遵循相關(guān)法規(guī)的前提下使用本指導(dǎo)原則�。
本指導(dǎo)原則是在現(xiàn)行法規(guī)���、標(biāo)準(zhǔn)體系及當(dāng)前認(rèn)知水平下制定的��,隨著法規(guī)、標(biāo)準(zhǔn)體系的不斷完善和科學(xué)技術(shù)的不斷發(fā)展�����,本指導(dǎo)原則相關(guān)內(nèi)容也將適時(shí)進(jìn)行調(diào)整�����。
一、適用范圍
本指導(dǎo)原則所指的醫(yī)用低溫保存箱是一個(gè)具有適當(dāng)容積和裝置的絕熱箱����,箱內(nèi)溫度可控制在-25℃~-164℃溫度區(qū)間內(nèi),用消耗電能的手段來制冷�,具有一個(gè)或多個(gè)間室。
本指導(dǎo)原則僅適用于采用蒸汽壓縮式制冷的醫(yī)用低溫保存箱�����。
處于其他溫度范圍的醫(yī)用低溫儲(chǔ)存設(shè)備可參考本指導(dǎo)原則�。
根據(jù)新《醫(yī)療器械分類目錄》(國(guó)家食品藥品監(jiān)督管理總局公告2017年第104號(hào)),分類編碼為22(臨床檢驗(yàn)器械)—15(檢驗(yàn)及其他輔助設(shè)備)—04(低溫儲(chǔ)存設(shè)備)��。
二���、技術(shù)審查要點(diǎn)
(一)產(chǎn)品名稱要求
產(chǎn)品的命名應(yīng)采用《醫(yī)療器械分類目錄》或國(guó)家標(biāo)準(zhǔn)�����、行業(yè)標(biāo)準(zhǔn)上的通用名稱����,或以產(chǎn)品結(jié)構(gòu)���、控制方式為依據(jù)命名����,應(yīng)符合《醫(yī)療器械通用名稱命名規(guī)則》(國(guó)家食品藥品監(jiān)督管理總局令第19號(hào))的要求。
建議使用的名稱有:低溫保存箱���、醫(yī)用低溫保存箱��、醫(yī)用冷凍箱等��。
(二)產(chǎn)品的結(jié)構(gòu)和組成
醫(yī)用低溫保存箱按門或蓋的打開形式可分為頂開式(臥式)和直立式(立式)���。
醫(yī)用低溫保存箱一般由圍護(hù)結(jié)構(gòu)、制冷系統(tǒng)���、控制系統(tǒng)����、數(shù)據(jù)記錄系統(tǒng)(可選配)及相關(guān)附件組成��。不同生產(chǎn)企業(yè)的產(chǎn)品��,在結(jié)構(gòu)上存在一定差異��,可不完全與本部分描述一致����。
1.圍護(hù)結(jié)構(gòu)用于醫(yī)用低溫保存箱的存儲(chǔ)空間結(jié)構(gòu)的組成及保溫。
2.制冷系統(tǒng)用于實(shí)現(xiàn)熱量的轉(zhuǎn)移����,使存儲(chǔ)空間內(nèi)維持所需求的溫度環(huán)境。
3.控制系統(tǒng)(可包括相應(yīng)軟件及獨(dú)立電源部分等)用于溫度等參數(shù)的監(jiān)控及供電���。
4.數(shù)據(jù)記錄系統(tǒng)(可選配)用于箱內(nèi)溫度或存儲(chǔ)樣品信息等的記錄��,包括打印機(jī)�、溫度記錄儀����、電子存儲(chǔ)設(shè)備等。
5.附件一般包括容器和擱架�����,也包括需用人工取出的盛物盤等���。
(三)產(chǎn)品工作原理/作用機(jī)理
1.產(chǎn)品以消耗電能的手段實(shí)現(xiàn)熱量的轉(zhuǎn)移����,從而主動(dòng)制造出所需的低溫環(huán)境。
蒸汽壓縮式制冷是指液態(tài)制冷劑在蒸發(fā)器中汽化變成氣態(tài)制冷劑進(jìn)入壓縮機(jī)�����,被壓縮成高溫高壓的氣體���,然后排放到冷凝器中����,在冷凝器的作用下��,氣態(tài)制冷劑被冷卻成高壓的液體�,然后進(jìn)入節(jié)流裝置(常見的有毛細(xì)管和膨脹閥),被節(jié)流的液態(tài)制冷劑的壓力和溫度再次降低����,液態(tài)制冷劑進(jìn)入蒸發(fā)器后,會(huì)再次汽化吸熱��,周而復(fù)始達(dá)到制冷效果����。
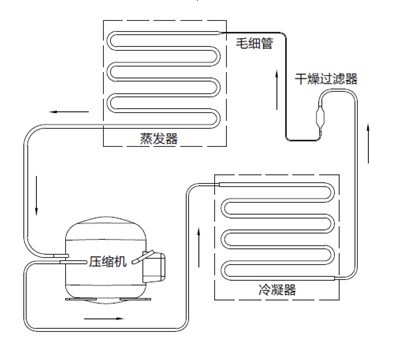
圖1 工作原理示意圖
2.因該產(chǎn)品為非治療類醫(yī)療器械,故本指導(dǎo)原則不包含產(chǎn)品作用機(jī)理的內(nèi)容����。
(四)注冊(cè)單元?jiǎng)澐值脑瓌t和實(shí)例
注冊(cè)單元?jiǎng)澐忠话阋援a(chǎn)品的技術(shù)原理、結(jié)構(gòu)組成���、性能指標(biāo)和適用范圍為劃分依據(jù)�。
原則上該指導(dǎo)原則涵蓋的產(chǎn)品可劃分為同一個(gè)注冊(cè)單元����。
(五)產(chǎn)品適用的相關(guān)標(biāo)準(zhǔn)
目前與產(chǎn)品相關(guān)的國(guó)家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)列舉如下:
表1 相關(guān)產(chǎn)品標(biāo)準(zhǔn)
GB/T 191—2008 | 包裝儲(chǔ)運(yùn)圖示標(biāo)志 |
GB 4706.13—2014 | 家用和類似用途電器的安全 制冷器具冰淇淋機(jī)和制冰機(jī)的特殊要求 |
GB 4793.1—2007 | 測(cè)量�����、控制和實(shí)驗(yàn)室用電氣設(shè)備的安全要求 第1部分:通用要求 |
GB/T 14710—2009 | 醫(yī)用電器環(huán)境要求及試驗(yàn)方法 |
GB/T 18268.1—2010 | 測(cè)量�、控制和實(shí)驗(yàn)室用的電設(shè)備 電磁兼容性要求 第1部分:通用要求 |
GB/T 20154—2014 | 低溫保存箱 |
YY/T 0316—2016 | 醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用 |
YY 0466.1—2016 | 醫(yī)療器械 用于醫(yī)療器械標(biāo)簽、標(biāo)記和提供信息的符號(hào) 第1部分:通用要求 |
上述標(biāo)準(zhǔn)包括了產(chǎn)品經(jīng)常涉及的標(biāo)準(zhǔn)�。有的企業(yè)還會(huì)根據(jù)產(chǎn)品的特點(diǎn)引用一些行業(yè)外的標(biāo)準(zhǔn)和一些較為特殊的標(biāo)準(zhǔn)。
產(chǎn)品適用及引用標(biāo)準(zhǔn)的審查可以分兩步來進(jìn)行����。首先對(duì)引用標(biāo)準(zhǔn)的齊全性和適宜性進(jìn)行審查,也就是在編寫產(chǎn)品技術(shù)要求時(shí)與產(chǎn)品相關(guān)的國(guó)家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)是否進(jìn)行了引用�����,以及引用是否準(zhǔn)確�。其次對(duì)引用標(biāo)準(zhǔn)的采納情況進(jìn)行審查。即所引用的標(biāo)準(zhǔn)中的條款要求���,是否在產(chǎn)品技術(shù)要求中進(jìn)行了實(shí)質(zhì)性的條款引用���。這種引用通常采用兩種方式,文字表述繁多�、內(nèi)容復(fù)雜的可以直接引用標(biāo)準(zhǔn)及條文號(hào),比較簡(jiǎn)單的也可以直接引述具體要求��。
如有新版強(qiáng)制性國(guó)家標(biāo)準(zhǔn)���、行業(yè)標(biāo)準(zhǔn)發(fā)布實(shí)施����,產(chǎn)品性能指標(biāo)等要求應(yīng)執(zhí)行最新版本的國(guó)家標(biāo)準(zhǔn)���、行業(yè)標(biāo)準(zhǔn)�。
(六)產(chǎn)品的適用范圍/預(yù)期用途、禁忌癥
用于提供低溫冷凍環(huán)境����,供醫(yī)療機(jī)構(gòu)儲(chǔ)存血漿等樣本。
產(chǎn)品無絕對(duì)禁忌癥��。
(七)產(chǎn)品研究要求
1.產(chǎn)品性能研究
應(yīng)當(dāng)提供產(chǎn)品性能研究資料以及產(chǎn)品技術(shù)要求的研究和編制說明��,包括功能性���、安全性指標(biāo)(如電氣安全與電磁兼容)以及與質(zhì)量控制相關(guān)的其他指標(biāo)的確定依據(jù),所采用的標(biāo)準(zhǔn)或方法���、采用的原因及理論基礎(chǔ)���。
研究資料中,需對(duì)醫(yī)用低溫保存箱產(chǎn)品所采用的制冷原理進(jìn)行詳細(xì)描述�,寫明制冷原理類型,如單級(jí)制冷系統(tǒng)��、雙級(jí)或多級(jí)復(fù)疊制冷系統(tǒng)�,應(yīng)列明工作原理框圖,并提供詳細(xì)的解釋說明��。需要對(duì)制冷系統(tǒng)所使用的制冷劑組分進(jìn)行描述,應(yīng)列明制冷劑制冷循環(huán)圖���、壓焓圖��,并提供詳細(xì)的解釋說明����。應(yīng)對(duì)預(yù)期冷凍的樣本提供相應(yīng)的描述及驗(yàn)證資料����。
2.消毒工藝研究
應(yīng)當(dāng)明確推薦的消毒工藝(方法和參數(shù))以及所推薦消毒方法的確定依據(jù)及必要的驗(yàn)證資料。
3.產(chǎn)品有效期和包裝研究
因各生產(chǎn)企業(yè)采用的原材料不同����,同時(shí)考慮到使用頻次的不同及一些不可預(yù)期的因素,產(chǎn)品的實(shí)際有效期會(huì)不同�����。應(yīng)對(duì)產(chǎn)品有效期進(jìn)行研究驗(yàn)證����。
產(chǎn)品經(jīng)環(huán)境試驗(yàn)和模擬運(yùn)輸試驗(yàn)驗(yàn)證,包裝應(yīng)符合運(yùn)輸和貯存的要求���。
4.軟件研究
參見《醫(yī)療器械軟件注冊(cè)技術(shù)審查指導(dǎo)原則》(國(guó)家食品藥品監(jiān)督管理總局通告2015年第50號(hào))的相關(guān)要求����。
對(duì)于具有網(wǎng)絡(luò)連接功能以進(jìn)行電子數(shù)據(jù)交換或遠(yuǎn)程監(jiān)測(cè)的產(chǎn)品,還應(yīng)當(dāng)按照《醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)技術(shù)審查指導(dǎo)原則》(國(guó)家食品藥品監(jiān)督管理總局通告2017年第13號(hào))單獨(dú)提交一份網(wǎng)絡(luò)安全描述文檔�。
5.其他資料
證明產(chǎn)品安全性、有效性的其他研究資料�����。
(八)產(chǎn)品的主要風(fēng)險(xiǎn)
1.醫(yī)用低溫保存箱的風(fēng)險(xiǎn)分析資料應(yīng)符合YY/T 0316—2016《醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用》的有關(guān)要求���,審查要點(diǎn)包括:
(1)識(shí)別醫(yī)療器械與安全有關(guān)特性的問題,可參考YY/T 0316—2016的附錄C����。
(2)危險(xiǎn)(源)、可預(yù)見的事件序列和危險(xiǎn)情況�����,可參考YY/T 0316—2016的附錄E����、I����。
(3)風(fēng)險(xiǎn)可接受準(zhǔn)則�,降低風(fēng)險(xiǎn)的措施及采取措施后風(fēng)險(xiǎn)的可接收程度,是否有新的風(fēng)險(xiǎn)產(chǎn)生�����。
(4)風(fēng)險(xiǎn)控制的方案與實(shí)施��、綜合剩余風(fēng)險(xiǎn)的可接受評(píng)價(jià)�,可參考YY/T 0316—2016的附錄F、G�、J。
2.根據(jù)YY/T 0316—2016的附錄E���,列舉了醫(yī)用低溫保存箱產(chǎn)品可能涉及的危險(xiǎn)(源)(見表2)����,企業(yè)還應(yīng)根據(jù)自身產(chǎn)品特點(diǎn)確定其他危險(xiǎn)(源)�����。針對(duì)產(chǎn)品的各項(xiàng)風(fēng)險(xiǎn)���,企業(yè)應(yīng)采取應(yīng)對(duì)措施�����,確保風(fēng)險(xiǎn)降到可接受的程度����。
表2 產(chǎn)品主要危險(xiǎn)(源)、可預(yù)見的事件序列和
可能發(fā)生的傷害之間的關(guān)系
危險(xiǎn)(源) | 可預(yù)見的事件序列 | 傷害 |
電能 | 保護(hù)接地阻抗����、可觸及部分的接觸電壓、電介質(zhì)強(qiáng)度不符合要求��; 機(jī)器外殼的防護(hù)罩封閉不良���;不適當(dāng)?shù)墓╇婋妷海浑姶偶嫒菪阅懿环弦蟆?/span> | 嚴(yán)重時(shí)導(dǎo)致操作人員觸電死亡�; 影響其他設(shè)備的正常運(yùn)轉(zhuǎn),導(dǎo)致人體傷害���。 |
熱能 | 操作人員不戴手套到箱內(nèi)存放或取出樣品�����。 | 可能造成操作人員凍傷�����。 |
機(jī)械 | 設(shè)備外殼粗糙���、有毛刺���;設(shè)備沒有足夠的外殼機(jī)械強(qiáng)度和剛度;機(jī)械穩(wěn)定性不夠����。 | 導(dǎo)致操作人員碰傷、擠傷�����、劃傷等傷害�。 |
噪聲 | 系統(tǒng)管路互碰或運(yùn)動(dòng)部件損壞;壓縮機(jī)噪聲��。 | 噪聲污染�。 |
化學(xué)物質(zhì) | 使用不適當(dāng)?shù)谋夭牧希恍铍姵剡_(dá)到壽命隨意丟棄�����。 | 污染環(huán)境。 |
功能 | 制冷劑泄露�、密封不良;軟件失效�����;實(shí)際儲(chǔ)存溫度與顯示板溫度不符���、故障提示異常����。 | 產(chǎn)品達(dá)不到預(yù)期使用溫度���,保存的產(chǎn)品失效。 |
人為因素 | 操作人員使用不當(dāng)����;軟件被誤操作、長(zhǎng)時(shí)間打開門或蓋以及忘記關(guān)門或蓋���。 | 保存產(chǎn)品的質(zhì)量受到影響���。 |
隨機(jī)信息 | 外部和內(nèi)部標(biāo)記不全面����、標(biāo)記不正確或不能夠清楚易認(rèn)���,標(biāo)記位置不恰當(dāng)����,以及標(biāo)記不能夠永久貼牢���;說明書缺少必要的警告說明和詳細(xì)的使用方法���;缺少詳細(xì)的日常使用維護(hù)規(guī)范;說明書中有關(guān)維護(hù)�、保養(yǎng)等內(nèi)容不明確。如:預(yù)防性檢查�����、保養(yǎng)以及保養(yǎng)周期等���;對(duì)設(shè)備的使用壽命或終止使用的條件沒有明確規(guī)定��。 | 保存產(chǎn)品的質(zhì)量受到影響���。 |
(九)產(chǎn)品技術(shù)要求應(yīng)包括的主要性能指標(biāo)
對(duì)產(chǎn)品的主要性能指標(biāo)的審查��,可以通過對(duì)檢驗(yàn)報(bào)告內(nèi)容的審查來評(píng)價(jià)是否達(dá)到了要求��,檢驗(yàn)報(bào)告的內(nèi)容是否齊全又可以通過對(duì)產(chǎn)品技術(shù)要求的內(nèi)容是否齊全來進(jìn)行審查���。因此產(chǎn)品技術(shù)要求的審查是產(chǎn)品主要技術(shù)性能指標(biāo)審查中最重要的環(huán)節(jié)之一。
可以通過是否具有以下主要內(nèi)容來進(jìn)行審評(píng)����。
1.規(guī)格型號(hào)
醫(yī)用低溫保存箱可按預(yù)期用途、結(jié)構(gòu)組成�、總有效容積、特性點(diǎn)溫度等分為不同規(guī)格型號(hào)���,可參照GB/T 20154—2014的規(guī)定����,如:DW—86L370表示—86℃��、立式���、總有效容積為370L的低溫保存箱���。
2.軟件信息
需對(duì)軟件名稱、型號(hào)規(guī)格���、發(fā)布版本��、完整版本命名規(guī)則作出規(guī)定�����。
3.一般性能
應(yīng)符合GB/T 20154—2014的技術(shù)要求����。
應(yīng)對(duì)附件制定相應(yīng)要求����,如容器、擱架���、需用人工取出的盛物盤��、溫度傳感器等����。
軟件功能應(yīng)符合說明書及軟件描述文檔中的功能描述。
若產(chǎn)品具有用以進(jìn)行電子數(shù)據(jù)交換或遠(yuǎn)程監(jiān)測(cè)的網(wǎng)絡(luò)連接功能���,應(yīng)制定相應(yīng)要求��。
超出本指導(dǎo)原則溫度范圍的醫(yī)用低溫保存箱可參考上述條款制定性能要求����。
4.安全性能
應(yīng)符合GB 4793.1—2007的要求����,并以附錄形式列明醫(yī)用實(shí)驗(yàn)室用電氣設(shè)備基本安全特征(無需編寫詳細(xì)的電氣安全附錄)。如需編寫詳細(xì)的電氣安全附錄����,建議注明適用項(xiàng)目及不適用項(xiàng)目理由。
5.電磁兼容
應(yīng)符合GB/T 18268.1—2010的要求�����。
6.環(huán)境試驗(yàn)
應(yīng)符合GB/T 14710—2009的要求���。
應(yīng)逐項(xiàng)審查上述要求和檢驗(yàn)結(jié)果是否符合規(guī)定����。
(十)同一注冊(cè)單元內(nèi)注冊(cè)檢驗(yàn)代表產(chǎn)品確定原則和實(shí)例
注冊(cè)檢驗(yàn)代表產(chǎn)品應(yīng)是同一注冊(cè)單元內(nèi)能夠代表本單元內(nèi)其他產(chǎn)品安全性和有效性的產(chǎn)品��,應(yīng)充分考慮產(chǎn)品功能��、結(jié)構(gòu)組成���、控制方式及產(chǎn)品其他風(fēng)險(xiǎn)等方面���。
注冊(cè)單元內(nèi)各型號(hào)的主要安全指標(biāo)、性能指標(biāo)不能被代表型號(hào)全部涵蓋時(shí)�����,則應(yīng)選擇涵蓋安全指標(biāo)����、性能指標(biāo)最多的產(chǎn)品作為代表產(chǎn)品,同時(shí)還應(yīng)考慮其他型號(hào)中未被代表型號(hào)所涵蓋的安全指標(biāo)及性能指標(biāo)�。
該產(chǎn)品代表型號(hào)的選擇應(yīng)著重考慮以下因素:結(jié)構(gòu)組成(如立式和臥式)、特性點(diǎn)溫度�、有效容積�、制冷原理類型���、關(guān)鍵元器件(如壓縮機(jī))等��。
此外���,產(chǎn)品在實(shí)施GB 4793.1—2007檢驗(yàn)時(shí),應(yīng)按照GB/T 18268.1—2010的要求實(shí)施電磁兼容檢驗(yàn)���。醫(yī)療器械檢驗(yàn)機(jī)構(gòu)對(duì)涉及電磁兼容性能的檢驗(yàn)出具檢驗(yàn)報(bào)告�����,對(duì)于檢驗(yàn)過程中發(fā)現(xiàn)的重大問題���,如基本性能判據(jù)、型號(hào)覆蓋等問題�,應(yīng)在檢驗(yàn)報(bào)告?zhèn)渥⒅性敿?xì)載明有關(guān)問題并注明自身意見,以供技術(shù)審查部門參考�����。電磁兼容檢驗(yàn)引起產(chǎn)品電氣安全發(fā)生變化的應(yīng)重新對(duì)電氣安全進(jìn)行檢驗(yàn)�����。
(十一)產(chǎn)品生產(chǎn)制造相關(guān)要求
應(yīng)當(dāng)明確產(chǎn)品生產(chǎn)工藝過程,可采用流程圖的形式�����,并說明其過程控制點(diǎn)��。
本類產(chǎn)品的關(guān)鍵過程一般包括發(fā)泡��、焊接���、抽空、灌注����、檢漏、產(chǎn)品測(cè)試檢驗(yàn)等�����。但當(dāng)上述過程中的一個(gè)或多個(gè)通過外包的方式來實(shí)現(xiàn)時(shí)�,生產(chǎn)企業(yè)應(yīng)對(duì)外包過程實(shí)施有效控制。
有多個(gè)研制����、生產(chǎn)場(chǎng)地���,應(yīng)當(dāng)分別明確每個(gè)研制、生產(chǎn)場(chǎng)地的生產(chǎn)制造和檢驗(yàn)等具體情況�。
(十二)產(chǎn)品的臨床評(píng)價(jià)細(xì)化要求
1.若注冊(cè)申報(bào)產(chǎn)品符合《免于進(jìn)行臨床試驗(yàn)的第二類醫(yī)療器械目錄》(國(guó)家食品藥品監(jiān)督管理總局通告2014年第12號(hào),以下簡(jiǎn)稱《目錄》)中“醫(yī)用低溫冰箱”的描述�����,則注冊(cè)申請(qǐng)時(shí)應(yīng)提交以下臨床評(píng)價(jià)資料:
(1)提交申報(bào)產(chǎn)品相關(guān)信息與《目錄》所述內(nèi)容的比對(duì)資料���,證明兩者具有等同性�����。
(2)提交申報(bào)產(chǎn)品與國(guó)內(nèi)已上市同品種醫(yī)療器械的比對(duì)說明�����,比對(duì)內(nèi)容包括基本原理����、所用材料、結(jié)構(gòu)組成���、性能指標(biāo)�、適用范圍���、使用方法等����,并提供必要的支持性資料���。
2.超出《目錄》中所述的溫度范圍的產(chǎn)品,可通過同品種醫(yī)療器械臨床試驗(yàn)或臨床使用獲得的數(shù)據(jù)進(jìn)行分析評(píng)價(jià)�����,并按照《醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則》(國(guó)家食品藥品監(jiān)督管理總局通告2015年第14號(hào))中相關(guān)要求提交臨床評(píng)價(jià)資料��?����;虬凑铡夺t(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則》和《醫(yī)療器械臨床試驗(yàn)質(zhì)量管理規(guī)范》(國(guó)家食品藥品監(jiān)督管理總局和國(guó)家衛(wèi)生和計(jì)劃生育委員會(huì)令第25號(hào))的要求提交臨床試驗(yàn)資料�。
(十三)產(chǎn)品的不良事件歷史記錄
該產(chǎn)品在上市后使用中出現(xiàn)的可疑不良事件主要有:箱門密封性不好、密封條老化�����;壓縮機(jī)、控溫器故障�;制冷劑泄漏等。
(十四)產(chǎn)品說明書和標(biāo)簽要求
產(chǎn)品說明書一般包括使用說明書和技術(shù)說明書��,兩者可合并��。說明書�、標(biāo)簽應(yīng)符合《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》(國(guó)家食品藥品監(jiān)督管理總局令第6號(hào))的要求,并參照GB/T 20154—2014和相應(yīng)國(guó)家標(biāo)準(zhǔn)�����、行業(yè)標(biāo)準(zhǔn)的要求進(jìn)行編寫��。還應(yīng)關(guān)注以下內(nèi)容:
1.產(chǎn)品適用范圍�、主要性能指標(biāo)、軟件發(fā)布版本���。
2.關(guān)于制冷原理的說明��、銘牌和圖示�。
3.關(guān)于產(chǎn)品安裝的說明。
4.對(duì)于產(chǎn)品使用方法���、產(chǎn)品壽命�����、維護(hù)保養(yǎng)等情況的說明��。
5.對(duì)于電磁兼容所聲稱的有關(guān)內(nèi)容(預(yù)期場(chǎng)所�、類別等)��。
6.對(duì)于安全性方面的注意事項(xiàng)�����,包括涉及低溫的潛在風(fēng)險(xiǎn)及安全措施�。
7.提示不要超出產(chǎn)品適用范圍使用��。
8.警示性說明����,如:不用于爆炸性環(huán)境,不可用于儲(chǔ)存可燃性物品���。
9.關(guān)于提醒使用者對(duì)冷凍效果進(jìn)行驗(yàn)證的警示說明����。
10.提示使用者對(duì)冷凍效果進(jìn)行監(jiān)測(cè)。
11.常見故障及排除方法����。
12.清潔/消毒方式。
13.制冷劑的種類和用量����,若使用碳?xì)渲评鋭鋯蜗到y(tǒng)用量必須符合安全用量標(biāo)準(zhǔn)�����,具體參見GB 4706.13—2014中22.106的要求�。
三、審查關(guān)注點(diǎn)
(一)產(chǎn)品電氣安全��、電磁兼容和主要性能指標(biāo)是否執(zhí)行了國(guó)家和行業(yè)的強(qiáng)制性標(biāo)準(zhǔn)����,是否引用了適用的推薦性標(biāo)準(zhǔn)。
(二)產(chǎn)品的主要風(fēng)險(xiǎn)是否已經(jīng)列舉��,并通過風(fēng)險(xiǎn)控制措施使產(chǎn)品的風(fēng)險(xiǎn)在合理可接受的水平之內(nèi)。
(三)臨床評(píng)價(jià)資料是否按照法規(guī)要求提供����。
(四)說明書是否符合《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》及相關(guān)國(guó)家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)的規(guī)定����。必須告知用戶的信息是否完整。說明書中建議提供突發(fā)事項(xiàng)的應(yīng)急預(yù)案����,如長(zhǎng)時(shí)間斷電等情況。因注冊(cè)申請(qǐng)人在對(duì)適用范圍內(nèi)所包含物品進(jìn)行冷凍效果驗(yàn)證時(shí)不可能涵蓋臨床層面所有可能因素���,故在說明書中應(yīng)提示使用者在使用前對(duì)冷凍效果進(jìn)行相應(yīng)驗(yàn)證����,并對(duì)其冷凍效果進(jìn)行實(shí)時(shí)監(jiān)測(cè)��。
(五)說明書��、標(biāo)簽必須標(biāo)明制冷劑的種類和用量����,若使用碳?xì)渲评鋭鋯蜗到y(tǒng)用量必須符合安全用量標(biāo)準(zhǔn)�,具體參見GB 4706.13—2014中22.106的要求。
四����、編寫單位
山東省食品藥品監(jiān)督管理局審評(píng)認(rèn)證中心。