如何決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)�?除了看免于進(jìn)行醫(yī)療器械臨床試驗(yàn)?zāi)夸?�,查看同類產(chǎn)品上市情況之外�����,總局發(fā)布的《決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)技術(shù)指導(dǎo)原則》同樣需要關(guān)注���。
如何決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)���?除了看免于進(jìn)行醫(yī)療器械臨床試驗(yàn)?zāi)夸?,查看同類產(chǎn)品上市情況之外���,總局發(fā)布的《決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)技術(shù)指導(dǎo)原則》同樣需要關(guān)注��。

決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)技術(shù)指導(dǎo)原則
決策是否開(kāi)展醫(yī)療器械臨床試驗(yàn)是綜合考慮產(chǎn)品的適用范圍���、技術(shù)特征、生物學(xué)特性����、風(fēng)險(xiǎn)程度及已有研究數(shù)據(jù)(包括臨床數(shù)據(jù)和非臨床數(shù)據(jù))等方面來(lái)確定開(kāi)展臨床試驗(yàn)必要性的過(guò)程。需要開(kāi)展臨床試驗(yàn)的����,可根據(jù)具體情況,選擇在境內(nèi)開(kāi)展臨床試驗(yàn)�����、全部或同期在境外開(kāi)展臨床試驗(yàn)����。
本指導(dǎo)原則旨在為注冊(cè)申請(qǐng)人和審查人員判斷擬申請(qǐng)注冊(cè)的產(chǎn)品是否需要開(kāi)展臨床試驗(yàn)提供技術(shù)指導(dǎo),不涉及注冊(cè)審批等行政事項(xiàng)�,亦不作為法規(guī)強(qiáng)制執(zhí)行����,如有能夠滿足法規(guī)要求的其他方法�����,也可以采用����,但應(yīng)提供詳細(xì)的研究資料和驗(yàn)證資料����。應(yīng)在遵循相關(guān)法規(guī)的前提下使用本指導(dǎo)原則。
一���、 適用范圍
本指導(dǎo)原則適用于需要開(kāi)展臨床評(píng)價(jià)的第二類�����、第三類醫(yī)療器械產(chǎn)品注冊(cè)時(shí)��,是否需要開(kāi)展臨床試驗(yàn)的判定�����,不適用于按醫(yī)療器械管理的體外診斷試劑��。
二����、總則
在醫(yī)療器械設(shè)計(jì)開(kāi)發(fā)過(guò)程中,設(shè)計(jì)確認(rèn)是其重要環(huán)節(jié)���,以確保產(chǎn)品能夠滿足規(guī)定的使用要求或者預(yù)期用途的要求����?�?刹扇《喾N方法實(shí)現(xiàn)設(shè)計(jì)確認(rèn)����,如模體試驗(yàn)、計(jì)算機(jī)模擬試驗(yàn)�、動(dòng)物試驗(yàn)、臨床評(píng)價(jià)等�。可用于臨床評(píng)價(jià)的臨床數(shù)據(jù)包括在境內(nèi)或境外�,合法的臨床使用過(guò)程中生成的安全性、有效性信息����,例如臨床試驗(yàn)數(shù)據(jù)�����、臨床文獻(xiàn)數(shù)據(jù)和臨床經(jīng)驗(yàn)數(shù)據(jù)等�。鼓勵(lì)注冊(cè)申請(qǐng)人采用最有效的方式獲取證明符合醫(yī)療器械安全和性能基本原則所需的最少量信息�����,消除或減輕不必要的負(fù)擔(dān)�,可使患者能夠及早并持續(xù)獲得安全有效的醫(yī)療器械���。臨床試驗(yàn)的必要性應(yīng)全面考慮醫(yī)療器械的適用范圍�、技術(shù)特征��、生物學(xué)特性���、風(fēng)險(xiǎn)程度��、與現(xiàn)有醫(yī)療器械或現(xiàn)有診療方法的差異等方面��,如果非臨床研究的結(jié)果和/或現(xiàn)有臨床數(shù)據(jù)不足以證明產(chǎn)品對(duì)醫(yī)療器械安全和性能的基本原則的符合性�,則可能需要開(kāi)展臨床試驗(yàn)?��;诹己迷O(shè)計(jì)和規(guī)范實(shí)施的臨床試驗(yàn)?zāi)軌蛱峁┛茖W(xué)��、可靠的醫(yī)療器械安全有效性數(shù)據(jù)�����。
本指導(dǎo)原則提到的符合醫(yī)療器械安全和性能基本原則����,是指對(duì)臨床證據(jù)與其他設(shè)計(jì)驗(yàn)證和確認(rèn)文件��、器械描述�、說(shuō)明書(shū)和標(biāo)簽、風(fēng)險(xiǎn)管理文件以及生產(chǎn)信息進(jìn)行綜合評(píng)價(jià)后得出的結(jié)論��。
三�、考慮因素
(一) 臨床使用具有高風(fēng)險(xiǎn)的第三類醫(yī)療器械(以下簡(jiǎn)稱“高風(fēng)險(xiǎn)醫(yī)療器械”),原則上需要開(kāi)展臨床試驗(yàn)�����,但以下情形可考慮免于開(kāi)展臨床試驗(yàn):
1.申報(bào)產(chǎn)品的前代產(chǎn)品未在中國(guó)獲準(zhǔn)上市,申報(bào)產(chǎn)品是對(duì)前代產(chǎn)品進(jìn)行的設(shè)計(jì)變更���,注冊(cè)申請(qǐng)人可通過(guò)已有數(shù)據(jù)(如非臨床研究數(shù)據(jù)�、前代產(chǎn)品的臨床試驗(yàn)數(shù)據(jù)�、申報(bào)產(chǎn)品境外臨床數(shù)據(jù))證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能基本原則。
2.注冊(cè)申請(qǐng)人可按照《接受醫(yī)療器械境外臨床試驗(yàn)數(shù)據(jù)技術(shù)指導(dǎo)原則》的要求提供申報(bào)產(chǎn)品境外臨床試驗(yàn)數(shù)據(jù)���,結(jié)合其他設(shè)計(jì)驗(yàn)證和確認(rèn)文件�����、器械描述����、說(shuō)明書(shū)和標(biāo)簽���、風(fēng)險(xiǎn)管理文件以及生產(chǎn)信息進(jìn)行綜合評(píng)價(jià),證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能的基本原則�����。
3.申報(bào)產(chǎn)品的前代產(chǎn)品已在中國(guó)獲準(zhǔn)上市�,申報(bào)產(chǎn)品是對(duì)前代產(chǎn)品進(jìn)行的設(shè)計(jì)變更,且注冊(cè)申請(qǐng)人可通過(guò)已有數(shù)據(jù)(如非臨床研究數(shù)據(jù)、前代產(chǎn)品的臨床數(shù)據(jù)��、申報(bào)產(chǎn)品境外臨床數(shù)據(jù))證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能基本原則�����。
前代產(chǎn)品是指與申報(bào)產(chǎn)品屬于同一注冊(cè)申請(qǐng)人���、具有相同適用范圍且技術(shù)特征和生物學(xué)特性相似的產(chǎn)品����,申報(bào)產(chǎn)品與前代產(chǎn)品為迭代關(guān)系��。
(二)申報(bào)產(chǎn)品雖然不屬于高風(fēng)險(xiǎn)醫(yī)療器械����,但為新型醫(yī)療器械,原則上應(yīng)開(kāi)展臨床試驗(yàn)���,但以下情形可考慮免于開(kāi)展臨床試驗(yàn):
1.注冊(cè)申請(qǐng)人可通過(guò)非臨床研究數(shù)據(jù)充分證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能基本原則�����。
2.申報(bào)產(chǎn)品在我國(guó)為新型醫(yī)療器械��,但其自身已有臨床數(shù)據(jù)(例如境外臨床文獻(xiàn)數(shù)據(jù)���、境外臨床試驗(yàn)數(shù)據(jù)等)���,注冊(cè)申請(qǐng)人可通過(guò)非臨床研究數(shù)據(jù)、申報(bào)產(chǎn)品的臨床數(shù)據(jù)證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能基本原則����。
3.申報(bào)產(chǎn)品在我國(guó)為新型醫(yī)療器械,但其前代產(chǎn)品已有境外臨床數(shù)據(jù)���,申報(bào)產(chǎn)品是對(duì)前代產(chǎn)品進(jìn)行的設(shè)計(jì)變更���,注冊(cè)申請(qǐng)人可通過(guò)非臨床研究數(shù)據(jù)、申報(bào)產(chǎn)品的境外臨床數(shù)據(jù)和前代產(chǎn)品的境外臨床數(shù)據(jù)充分證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能基本原則��。
新型醫(yī)療器械是指與已在中國(guó)境內(nèi)獲準(zhǔn)上市的醫(yī)療器械相比���,在適用范圍、技術(shù)特征和/或生物學(xué)特性等方面具有顯著差異的醫(yī)療器械�。大部分醫(yī)療器械是一個(gè)漸進(jìn)的變更過(guò)程,并不屬于新型醫(yī)療器械,很多情形下��,可以通過(guò)非臨床研究來(lái)證明其符合醫(yī)療器械安全和性能的基本原則。
(三)產(chǎn)品不屬于高風(fēng)險(xiǎn)醫(yī)療器械��,也不屬于新型醫(yī)療器械���,在注冊(cè)申請(qǐng)人已開(kāi)展充分的非臨床研究且全面收集已有臨床數(shù)據(jù)的基礎(chǔ)上����,若已有證據(jù)不能證明產(chǎn)品符合醫(yī)療器械安全和性能的基本原則時(shí)�,有可能需要通過(guò)開(kāi)展臨床試驗(yàn)補(bǔ)充臨床數(shù)據(jù)。獲得的臨床試驗(yàn)數(shù)據(jù)用于產(chǎn)品臨床評(píng)價(jià)過(guò)程且為臨床證據(jù)的一部分���。
例如��,對(duì)于特定申報(bào)產(chǎn)品���,其已有同品種產(chǎn)品在中國(guó)獲準(zhǔn)注冊(cè),申報(bào)產(chǎn)品與同品種產(chǎn)品存在差異�。若注冊(cè)申請(qǐng)人基于申報(bào)產(chǎn)品的非臨床研究數(shù)據(jù)以及同品種產(chǎn)品的臨床數(shù)據(jù)對(duì)產(chǎn)品實(shí)施了全面的臨床評(píng)價(jià),但仍不能證明申報(bào)產(chǎn)品符合醫(yī)療器械安全和性能的基本原則�����,則可能需要開(kāi)展臨床試驗(yàn)�����。
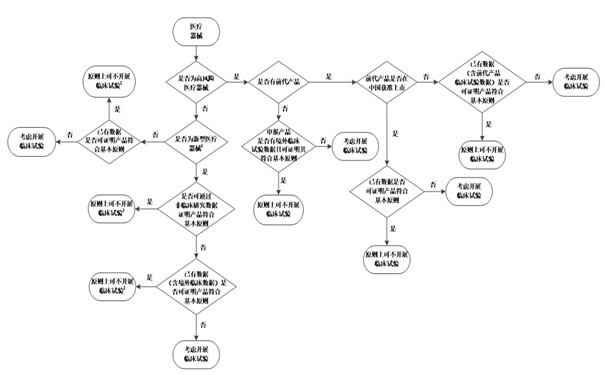
當(dāng)注冊(cè)申請(qǐng)人根據(jù)以上因素考慮是否開(kāi)展醫(yī)療器械臨床試驗(yàn)時(shí),可參考《醫(yī)療器械臨床試驗(yàn)決策流程圖》���。
附件:醫(yī)療器械臨床試驗(yàn)決策流程圖